氢气和氮气反应方程式 是吸热还是放热
放热反应。氮气与氢气的反应是工业制氨气的重要方法,高二的化学会学到。方程式为:N2(g)+3H2(g)=(催化剂,加热加压)2NH3(g);ΔH=-92.4kJ/mol,催化剂是铁触媒,该反应为可逆反应。

氢气和氮气反应放热
N?(g)+3H?(g)→2NH?(g) △H=-92.4kJ/mol,由此可知是放热反应。(在热化学方程式中,若为放热反应,则△H为“-”;若为吸热反应,则△H为“+”)
氨合成将纯净的氢、氮混合气压缩到高压,在催化剂的作用下合成氨。氨合成反应在较高压力和催化剂存在的条件下进行,由于反应后气体中氨含量不高,一般只有100故采用未反应氢氮气循环的流程。
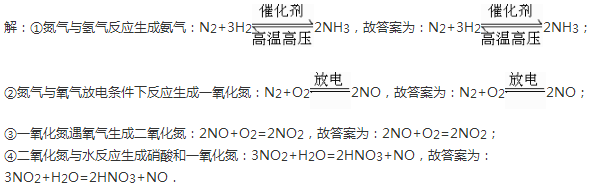
写出下列反应方程式
(注意反应发生的条件)
①氮气与氢气:______;
②氮气与氧气:______;
③NO和O2:______;
④NO2和水:______.